Neuroscience Department
ΕΡΕΥΝΑ, Πολλαπλή Σκλήρυνση και κονεξίνες

Η πολλαπλή σκλήρυνση (ΠΣ) ή σκλήρυνση κατά πλάκας, είναι μία αυτοάνοση, νευρολογική νόσος που προσβάλει το κεντρικό νευρικό σύστημα (ΚΝΣ), το οποίο απαρτίζεται από τον εγκέφαλο και τον νωτιαίο μυελό. Η νόσος παρουσιάζει διαφορετική κλινική πορεία από ασθενή σε ασθενή και μπορεί να οδηγήσει σε αναπηρία. Στην ΠΣ, τα λευκά κύτταρα του αίματος εισέρχονται στο ΚΝΣ και επιτίθενται λανθασμένα στην μυελίνη που είναι το προστατευτικό κάλυμμα των νευρώνων, όπως είναι το πλαστικό κάλυμμα στα ηλεκτρικά καλώδια. Η μυελίνη προσφέρει προστασία στους νευρώνες και βοηθά στη γρήγορη μετάδοση των νευρικών ώσεων, κι έτσι η πρόκληση πολλαπλών ουλών (σκλήρυνση) πάνω στην μυελίνη κάνει ευάλωτους τους νευρώνες και δυσχεραίνει την λειτουργία τους. Για την μελέτη της ΠΣ στο εργαστήριο, προκαλείται πειραματικώς σε ζώα πειραματική αυτοάνοση εγκεφαλομυελίτιδα (ΠΑΕ), μία νόσος της οποίας η κλινική εικόνα και τα συμπτώματα ομοιάζουν με αυτά της ΠΣ.
Ο ρόλος και η δομή του αιματεγκεφαλικού φραγμού, και η συσχέτισή του με την πολλαπλή σκλήρυνση
Ο αιματεγκεφαλικός φραγμός λειτουργεί σαν ένα ημι-διαπερατό φράγμα μεταξύ του αίματος και του ΚΝΣ, και εμποδίζει την επικίνδυνη εισχώρηση ουσιών και κυττάρων του αίματος μέσα στο ΚΝΣ. Σε περίπτωση που διαταραχθεί η ακεραιότητα του αιματεγκεφαλικού φραγμού και εισχωρήσουν ουσίες και λευκά κύτταρα του αίματος στο ΚΝΣ, τότε προκαλούνται νευρολογικές ασθένειες όπως η ΠΣ.
Οι κονεξίνες και ο ρόλος τους
Οι κονεξίνες είναι πρωτεΐνες και συμβάλλουν στην κατασκευή πρωτεϊνικών διαύλων (ή χασμοσυνδέσμων), οι οποίοι επιτρέπουν την ανταλλαγή ουσιών και την επικοινωνία μεταξύ των κυττάρων (Εικόνα 1). Συγκεκριμένα, έξι μόρια κονεξίνης δομούν έναν εξαμερή πρωτεϊνικό ημι-δίαυλο (ή κονεξόνιο), και δύο πρωτεϊνικοί ημι-δίαυλοι δομούν έναν πρωτεϊνικό δίαυλο (ή χασμοσύνδεσμο). Οι κονεξίνες εκφράζονται σε όλα τα κύτταρα αλλά κάθε κύτταρο εκφράζει διαφορετικό τύπο κονεξίνης. Στο ΚΝΣ, τα ολιγοδενδροκύτταρα (τα κύτταρα που παράγουν την μυελίνη των νευρώνων) παράγουν τις κονεξίνες 32 (ΚΞ32) και 47 (ΚΞ47) που επιτρέπουν την ανταλλαγή ουσιών μεταξύ των ολιγοδενδροκυττάρων, και μεταξύ ολιγοδενδροκυττάρων και αστροκυττάρων (κύτταρα του ΚΝΣ που συμβάλλουν στην θρέψη και προστασία των νευρώνων).
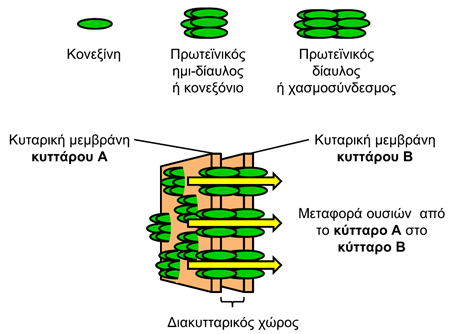
Εικόνα 1. Σχηματική απεικόνιση των κονεξινών και των πρωτεϊνικών διαύλων που σχηματίζουν, εξασφαλίζοντας την ανταλλαγή ουσιών και την επικοινωνία μεταξύ των κυττάρων.
Συσχέτιση των κονεξινών 32 και 47 με την πολλαπλή σκλήρυνση
Για την μελέτη του ρόλου που διαδραματίζουν οι ΚΞ32 και ΚΞ47 κατά την νόσηση με ΠΣ, προκλήθηκε ΠΑΕ σε φυσιολογικά ποντίκια και σε γενετικώς τροποποιημένα ποντίκια, τα οποία παρουσιάζουν παντελή έλλειψη της ΚΞ32 (χωρίς-ΚΞ32 ποντίκια), είτε παντελή έλλειψη της ΚΞ47 (χωρίς-ΚΞ47 ποντίκια).
Από τα αποτελέσματα της πειραματικής έρευνας που διεξήχθη πρόσφατα στο εργαστήριό μας, διαπιστώθηκε ότι τα χωρίς-ΚΞ47 ποντίκια με ΠΑΕ παρουσιάζουν πιο σοβαρή εξέλιξη της νόσου, και εκδηλώνουν τα πρώτα συμπτώματα αρκετά νωρίτερα από τα φυσιολογικά ποντίκια με ΠΑΕ και τα χωρίς-ΚΞ32 ποντίκια με ΠΑΕ. Επιπλέον, τα χωρίς-ΚΞ47 ΠΑΕ ποντίκια παρουσίασαν σοβαρότερη φλεγμονή στο ΚΝΣ συγκριτικά με τα υπόλοιπα ποντίκια. Πριν την εμφάνιση των πρώτων συμπτωμάτων της νόσου , τα χωρίς-ΚΞ47 ΠΑΕ ποντίκια είχαν ασθενέστερο αιματεγκεφαλικό φραγμό. Ως εκ τούτου, παρουσιάστηκε υψηλότερη διείσδυση Τ-λεμφοκυττάρων (τύπος λευκών κυττάρων του αίματος) στο ΚΝΣ, καθιστώντας τα ποντίκια αυτά πιο επιρρεπή στην νόσο.
Όλα τα πιο πάνω ευρήματα δείχνουν ότι η ΚΞ47, και σε μικρότερο βαθμό η ΚΞ32, είναι πολύ σημαντική για την φυσιολογική λειτουργία του ΚΝΣ και η απουσία της κάνει το ΚΝΣ πιο επιρρεπές στην νόσηση με ΠΑΕ, και επομένως με ΠΣ. Αυτό, επίσης διαφαίνεται σε προηγούμενες μελέτες του εργαστηρίου μας, όπου σε εγκεφάλους ασθενών με ΠΣ, έχουν βρεθεί μειωμένα επίπεδα των ΚΞ47 και ΚΞ32 κοντά και πέριξ των ουλών που προκλήθηκαν από ΠΣ. Περαιτέρω ανάλυση της λειτουργίας της ΚΞ47 θα βοηθήσει στο να ανακαλυφθούν μηχανισμοί που εμπλέκονται στην παθογένεση της ΠΣ. Συμπερασματικά, το ερευνητικό μας έργο έχει τεράστιο επιστημονικό και ιατρικό όφελος, όχι μόνο εθνικής αλλά και διεθνούς σημασίας, αφού η κατανόηση της πάθησης θα ανοίξει προοπτικές θεραπευτικής προσέγγισής της.
Λεπτομερής περιγραφή της πειραματικής έρευνας έχει δημοσιευθεί στο επιστημονικό περιοδικό Pharmaceuticals το 2021, με τίτλο «Dysregulation of Blood-Brain Barrier and Exacerbated Inflammatory Response in Cx47-Deficient Mice after Induction of EAE»
Άρθρο
Φίλιππος Σταυρόπουλος
Διδακτορικός φοιτητής, Σχολή Μοριακής Ιατρικής Κύπρου
Τμήμα Νευροεπιστημών










0002.jpg)
